Faktoren für das Therapieansprechen auf Brentuximab vedotin beim kutanen T-Zell Lymphom
Dieses Projekt wurde 2024 von der Stiftung "Forschung hilft" mit 10.000 Euro gefördert.

Abbildung 1: Wissenschaftliche Arbeitsgruppe "Kutane Lymphome" der Universitätshautklinik
Team
In der Arbeitsgruppe "Kutane Lymphome" beschäftigen wir uns seit vielen Jahren mit den molekularen Veränderungen bei Hautlymphomen. Darauf basierend untersuchen wir Möglichkeiten, die Diagnostik von Hautlymphomen und insbesondere die Therapie bei fortgeschrittenen Stadien dieser Erkrankung zu optimieren. Unter der Leitung von Prof. Dr. med. Marion Wobser setzt sich das Team aus erfahrenen Biologen, Ärzten, Doktoranden und technischen Assistenten zusammen.
Motivation und Innovation
Patienten in fortgeschrittenen Stadien von Hautlymphomen zeigen eine deutliche Beeinträchtigung der Lebensqualität, ein häufig nur kurzfristiges Ansprechen auf bisherige Behandlungsmaßnahmen und eine reduzierte Lebenserwartung. Somit ist eine Verbesserung der zur Verfügung stehenden Therapieoptionen von fundamentalem Interesse. Dieses Ziel steht im Zentrum unserer translational ausgerichteten Forschungsarbeiten. „Forschung hilft“ ist das wunderbare Motto der Stiftung zur Förderung der Krebsforschung an unserer Universität. In der Tat ist die Grundlagenforschung der Motor, der den Fortschritt in der Medizin antreibt, und wir wären dankbar, einen Beitrag dazu mit unserem Team aus Grundlagenwissenschaftlern, technischen Assistenten und Ärzten leisten zu dürfen.
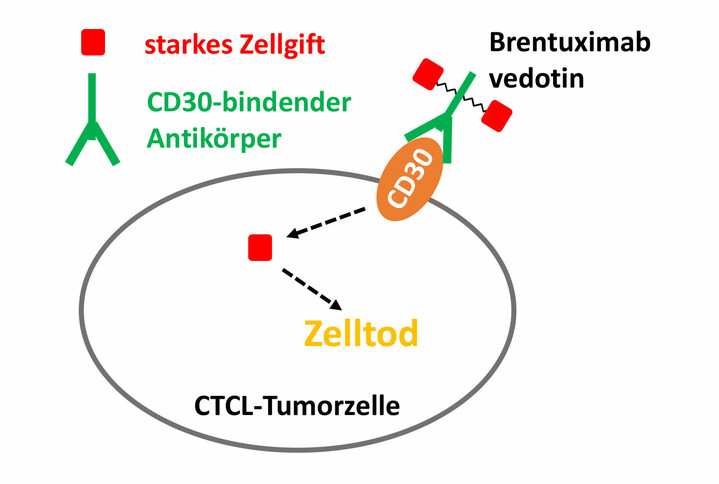
Abbildung 2: Wirkmechanismus von Brentuximab vedotin
Brentuximab vedotin (BV) besteht aus einem monoklonalen Antikörper, an den ein Zellgift (MMAE) gekoppelt ist. Der Antikörper bindet an CD30. CD30 ist ein Oberflächenmolekül, das von vielen kutanen T Zell-Lymphomzellen exprimiert wird. Nach erfolgter Bindung wird das Immunkonjugat von der CD30 positiven Tumorzelle aufgenommen, das Zellgift in der Zelle freigesetzt, welches dann zum Tod der Tumorzelle führt.
Welche Ziele verfolgt das Projekt?
Brentuximab vedotin (BV; Adcetris™) ist ein für das kutane T-Zelllymphom (CTCL) zugelassenes Therapeutikum. Dieses nutzt das Vorhandensein eines bestimmten Eiweißmoleküls (=CD30) auf der Oberfläche der Tumorzellen, um einen toxischen Wirkstoff ganz gezielt in die Tumorzellen einzubringen (Abb. 2).
Diese Therapie erweist sich für diejenigen CTCL Subtypen als hochwirksam, bei denen alle Tumorzellen eines Patienten CD30 stark exprimieren. Dies ist aber für andere Subtypen nicht gegeben. Bei diesen ist der Grad der CD30-Positivität - bestimmt mittels Immunhistochemie an Gewebsmaterial - ein unzureichender Marker für das Therapieansprechen gegenüber BV. Ein möglicher Grund dafür ist, dass Tumorzellen mit geringer CD30-Expression mit dieser Methode nicht detektiert werden können. Mittels einer neuartigen Methode (spatial transcriptomics; siehe unten) wollen wir dies überprüfen und darüber hinaus insbesondere auch Faktoren identifizieren, welche die Expression von CD30 im CTCL regulieren können. Basierend auf unseren Erkenntnissen versprechen wir uns, in Zukunft durch eine entsprechend angepasste Therapie mit BV eine bessere Wirksamkeit zu erzielen und somit noch mehr Lymphom-Patienten zu helfen.
Ansatz des Forschungsprojektes
Aus Zellkulturexperimenten wissen wir, dass die Effizienz von BV vom Expressionsniveau von CD30 abhängt. Dagegen scheint die Bestimmung der Frequenz an CD30-positiven Zellen durch Immunhistochemie kein guter Marker für das Therapieansprechen von Patienten mit Hautlymphomen gegenüber BV zu sein. Wir wollen Tumorgewebe von Patienten untersuchen, die unterschiedlich auf eine BV-Therapie angesprochen haben. Dabei kommt die hochmoderne Technik der spatial transcriptomics zum Einsatz, mit der die räumliche Verteilung der Expression aller Gene in Geweben erfasst werden kann. Dies ermöglicht es uns, die Aktivität von Genen in verschiedenen Bereichen eines Gewebes zu kartieren und somit folgende Punkte zu verstehen:
- wie ist das Expressionsniveau von CD30 verteilt,
- welche Faktoren führen zu einer bestimmten Ausprägung (wie einer Expression von CD30) und
- wie kommunizieren Zellen miteinander im Tumor.
Zentrales Ziel unserer Untersuchungen ist es, die Regulation und die Rolle der CD30 Expression sowie mögliche Resistenzmechanismen gegenüber BV beim CTCL besser zu verstehen und Faktoren für das Therapieansprechen auf BV zu identifizieren.
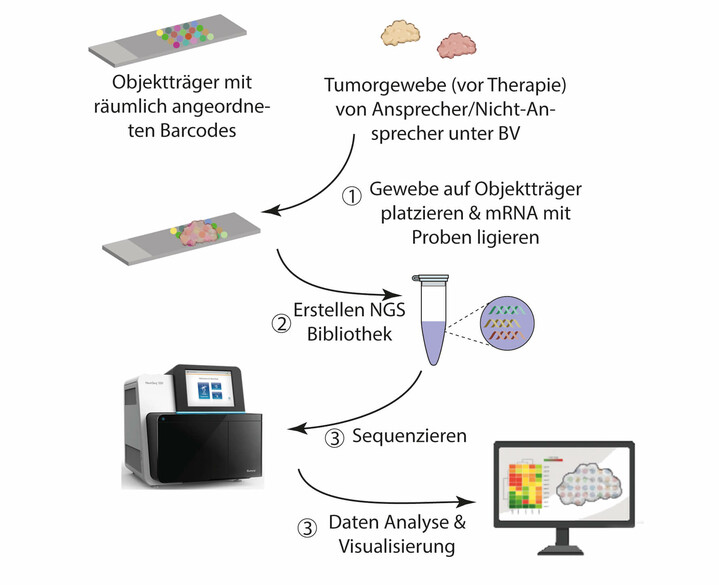
Abbildung 3: Das Prinzip der spatial transcriptomics.
Welche Krebserkrankung soll behandelt werden?
Das kutane T-Zell-Lymphom (CTCL) ist eine von bestimmten Zellen des Immunsystems, nämlich den T-Zellen, ausgehende, sich in der Haut manifestierende Tumorerkrankung. Das CTCL umfasst eine Gruppe verschiedener Krankheiten, darunter die Mycosis fungoides und das Sézary-Syndrom, die sich in Symptomen, Verlauf und Prognose unterscheiden können. Ein CTCL beginnt oft mit unspezifischen Hautveränderungen wie roten, schuppigen und juckenden Flecken. Im Verlauf können sich diese Läsionen zu Plaques oder Tumoren entwickeln und sich auch großflächig am Körper manifestieren. Während das CTCL meist langsam fortschreitet und auf die Haut beschränkt bleibt, kann sich die Erkrankung bei Patienten mit aggressivem Verlauf auch in Blut und innere Organe ausbreiten und tödlich enden. Die Behandlung hängt vor allem vom Krankheitsstadium ab, und in fortgeschrittenen Stadien kommen verschiedene Systemtherapien (Immuntherapie, Chemotherapie, Radiotherapie) und in Einzelfällen auch eine Stammzelltransplantation zum Einsatz. Die Prognose variiert je nach Subtyp, Krankheitsstadium und Ansprechen auf die Behandlung. Häufig zeigen sich rasch Krankheitsrückfälle nach erfolgter Therapie, sodass eine Verbesserung der zur Verfügung stehenden Therapieoptionen von vordergründigem Interesse ist.
Warum soll das Forschungsprojekt unterstützt werden?
Wenn im CTCL von allen Tumorzellen CD30 exprimiert wird, steht uns mit BV eine zielgerichtete, hocheffektive Therapie auch für fortgeschrittene Stadien zur Verfügung. Wenn wir nun den ursächlichen Unterschied zwischen den CD30-exprimierenden und nicht-exprimierenden Zellen verstehen, gewinnen wir translational bedeutende Schlüsselerkenntnisse, wie wir die CD30 Expression so stimulieren können, dass die Erfolgsrate der BV-Therapie beim CTCL entscheidend gesteigert werden kann. Im vorgeschlagenen Projekt wollen wir für die genannte Fragestellung die hochmoderne Analysemethode der „spatial transcriptomics“ zur Anwendung bringen. Der zentrale Antrieb für unsere wissenschaftlichen Arbeiten ist das gemeinsame Bestreben unseres Forschungsteams, CD30-basierte zielgerichtete Therapieansätze durch diese Erkenntnisse so zu optimieren, dass wir in Zukunft das Therapieansprechen verbessern und folglich die Lebensdauer von Patienten mit CTCL verlängern können.
